2016三大类医疗器械将不再享受备案后直接上市
发表日期:2016-01-04
1月4日讯 医械圈内的人都知道第一类医械在医械圈内很吃香,因为国家2014年6月1日发布了《医疗器械监督管理条例》开始实施,将第一类医疗器械上市许可由原来的注册审批制改为备案制。也就是说凡是在《第一类医疗器械产品目录》内的第一类医疗器械只需要备案后即可上市,无需注册。这样就免除了注册费的成本。
2015年7月配套发布了《医疗器械分类规则》(国家食品药品监管总局令第15号),新分类将于2016年1月1日起施行,围绕一类目录及豁免临床的二类、三类产品,对结构组成、预期用途等都加上了较为具体和细致的描述,企业在使用目录时不能像过去仅从产品名称出发,而应从产品属性出发,即工程原理、分类规则的要素等,寻找产品在目录中的正确位置。
同时,CFDA还规定本规则自2016年1月1日起施行。2000年4月5日公布的《医疗器械分类规则》(原国家药品监督管理局令第15号)同时废止。
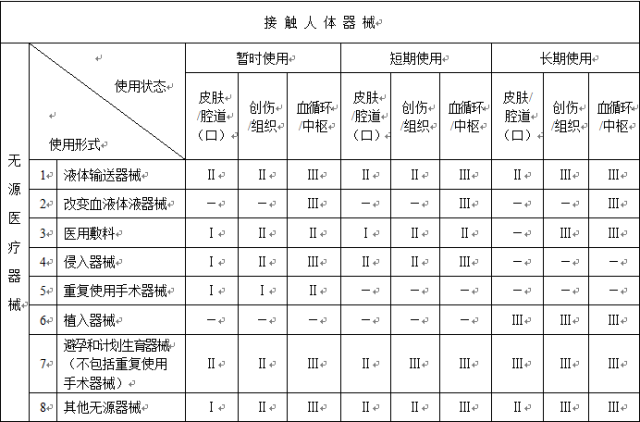
以下是按照新的《医疗器械分类规则》整理的分类判定表
上一篇: 老龄化社会施压医保支出 医保改革不能止步个人缴费
下一篇: 社区医院常用药有点儿缺 居民最盼增加药品种类
热门文章排行
更多>>
- 联合国秘书长呼吁停止歧视自...
- 重庆居民慢性病自我管理组首...
- 医学期刊表现抢眼 我国学术...
- 2010年6个医学相关学科取得...
- 听障和脑瘫抢救性门诊费实现...
- 七部门联合检查 所有医疗机...
- 青岛联动机制智斗非法行医“...
- 湖北重点地方病防治“答卷”...
- 山西6月底前实现城镇医保市...
- 零差价冲击客源 单体药店或...
- 医学类毕业生就业冷热不均
- 医药职专就业:畅通“出口”...
- 上海五年内将对儿科、产科、...
- 硕士去绍兴就业 购房打6折
- 应届毕业生春季招聘进入倒计...
- 学历门槛成了就业拦路虎
- 县级医院发展势头猛 医疗人...
- 首批医疗监督大使给力民营医...
- 全球每年死产婴儿数降幅仅1....
- 卫生信息化发力 公私医院实...







